Chuyện trên đường
22/11/2020 20:33Mỹ cấp phép sử dụng khẩn cấp loại thuốc từng điều trị COVID-19 cho ông Trump
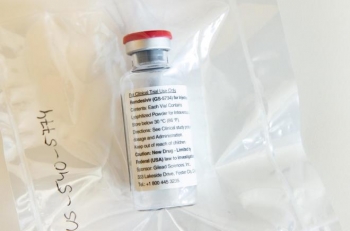
Cục quản lý Thực phẩm và Dược phẩm (FDA) của Mỹ cho phép sử dụng khẩn cấp thuốc của công ty Regeneron Pharmaceuticals với bệnh nhân COVID-19. Loại thuốc này ngăn COVID-19 trở nặng hơn ở những bệnh nhân có triệu chứng từ nhẹ đến trung bình, nhằm giảm tỷ lệ người nhập viện trong đại dịch.
 |
| FDA cho phép sử dụng khẩn cấp thuốc của công ty Regeneron Pharmaceuticals với bệnh nhân COVID-19. (Ảnh: AP) |
Đây là loại thuốc dùng điều trị một lần. FDA cấp phép sử dụng thuốc này với người lớn, trẻ em từ 12 tuổi trở lên nặng ít nhất (40 kg) và những bệnh nhân COVID-19 lớn tuổi hoặc có bệnh nền.
Thuốc được sử dụng trong khi các công ty dược phẩm vẫn tiếp tục thử nghiệm tính an toàn và hiệu quả của vaccine COVID-19.
Công ty Regeneron Pharmaceuticals cho biết đợt thuốc đầu tiên sẽ được cung cấp cho khoảng 300.000 bệnh nhân thông qua chương trình phân phối của chính phủ liên bang. Bệnh nhân được miễn phí thuốc nhưng có thể phải trả một phần chi phí tiêm. Lượng thuốc ban đầu có khả năng không đáp ứng đủ nhu cầu sử dụng do số ca nhiễm tại Mỹ đã vượt quá 12 triệu người.
Các chuyên gia y tế Mỹ cảnh báo nước này còn phải đối mặt với một mùa đông khắc nghiệt do không kiểm soát được sự lây lan của virus SARS-CoV-2. Hiện vẫn chưa thể xác định thuốc của Regeneron có phải là nguyên nhân giúp Tổng thống Trump hồi phục hay không do ông được tiếp nhận nhiều phương pháp điều trị khác nhau.
Các nhà quản lý của FDA cũng cho phép công ty Regeneron sử dụng quyền hạn khẩn cấp để đẩy nhanh tốc độ phát triển của các loại thuốc thử nghiệm cùng những sản phẩm y tế khác trong cuộc khủng hoảng vì đại dịch.
Thông thường, FDA sẽ yêu cầu “bằng chứng xác đáng” để chứng minh thuốc đảm bảo tính an toàn và hiệu quả trước khi cấp phép đưa vào sử dụng. Loại thuốc đó sẽ cần thông qua một hoặc nhiều thử nghiệm lớn được kiểm soát chặt chẽ. Nhưng trong trường hợp khẩn cấp, cơ quan này có thể hạ thấp tiêu chuẩn. Thay vì phải qua quá trình kiểm tra phức tạp, phương pháp điều trị thử nghiệm chỉ cần có lợi ích tiềm năng lớn hơn rủi ro là đủ.
Quyết định cho phép sử dụng khẩn cấp có chức năng tương tự sự chấp nhận tạm thời trong thời gian diễn ra đại dịch COVID-19.
Để có giấy phép chấp nhận hoàn toàn, Regeneron Pharmaceuticals cần cung cấp thêm nhiều kết quả nghiên cứu có thể xác nhận tính an toàn và hiệu quả điều trị của thuốc.
 |
Trước bầu cử tổng thống, Mỹ lần đầu công bố thuốc điều trị COVID-19
Thuốc Remdesivir của công ty dược Gilead đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) chấp thuận điều trị cho ... |
 |
Kháng thể Regeneron “đắt hàng” sau sự hồi phục siêu nhanh của Tổng thống Donald Trump
Nhu cầu được điều trị bằng kháng thể thử nghiệm Regeneron đang tăng lên chóng mặt sau khi sức khỏe của Tổng thống Mỹ Donald ... |








- Sự xuất hiện của siêu AI đưa cuộc săn lùng người ngoài hành tinh bước sang chương mới đầy chấn động (31/05/26 21:31)
- “Ốc mượn hồn” và kỳ vọng giữ nhiệt cho phim Việt mùa hè (31/05/26 18:48)
- Vietjet mở đường bay Nha Trang – Singapore trước sự chứng kiến của Tổng Bí thư, Chủ tịch nước Tô Lâm (31/05/26 17:30)
- Bill Gates hoen ố hình tượng vì hơn 20 mối quan hệ ngoài luồng, sắp phải ra trình diện trước quốc hội (31/05/26 17:21)
- Thống kê 'khủng' của Paris Saint-Germain sau chức vô địch Champions League (31/05/26 17:04)
- WHO chạy đua ngăn Ebola bùng phát tại Congo (31/05/26 17:02)
- Lầu Năm Góc để ngỏ khả năng tái tấn công Iran (31/05/26 16:54)
- Lịch công bố điểm thi, điểm chuẩn lớp 10 Hà Nội năm 2026 chính thức (31/05/26 16:49)
- Chứng khoán dự báo còn rung lắc, nhà đầu tư nên làm gì? (31/05/26 16:48)
- Nhan sắc nóng bỏng của mỹ nhân Colombia đăng quang Miss Grand All Stars (31/05/26 16:42)







