Sống khỏe
24/01/2022 14:45Đã phân bổ hơn 450.000 liều thuốc Molnupiravir điều trị F0 thể nhẹ
Trước đó, vào tháng 8/2021, Bộ Y tế đã triển khai điều trị thí điểm thuốc Molinupiravir tại TP Hồ Chí Minh và một số tỉnh, thành phố phía Nam. Trên cơ sở kết quả những nghiên cứu thử nghiệm lâm sàng thuốc Molnupiravir cho thấy tính an toàn và hiệu quả của thuốc, Bộ Y tế đã chỉ đạo các đơn vị nghiên cứu (Bệnh viện Phổi Trung ương, Đại học Y Dược TP Hồ Chí Minh) phối hợp với các Sở Y tế để triển khai Chương trình thí điểm điều trị có kiểm soát thuốc Molnupiravir cho các trường hợp mắc COVID-19 thể nhẹ.
Các kết quả báo cáo giữa kỳ của chương trình tại 22 tỉnh/thành phố cho thấy thuốc Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân... Những người không sử dụng thuốc kháng virus này gồm người bệnh quá mẫn hoặc chống chỉ định với thuốc, tiền sử mắc virus viêm gan B hoặc C kèm xơ gan, bệnh gan giai đoạn cuối, ung thư biểu mô tế bào gan, tiền sử viêm tụy cấp, viêm tụy mạn, tổn thương thận cấp hoặc suy thận nặng, phụ nữ có thai, đang cho con bú...
 |
T.H
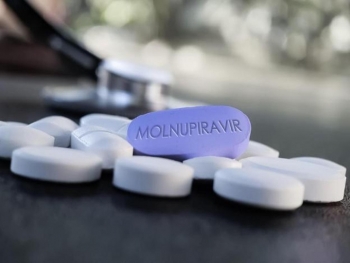 Bộ Y tế cảnh báo thuốc Molnupiravir ảnh hưởng đến tinh trùng Bộ Y tế cảnh báo thuốc Molnupiravir ảnh hưởng đến tinh trùng |
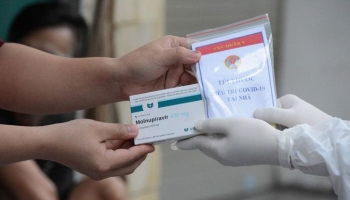 Người Hà Nội lùng mua thuốc Molnupiravir để tích trữ, Bộ Y tế yêu cầu xử lý Người Hà Nội lùng mua thuốc Molnupiravir để tích trữ, Bộ Y tế yêu cầu xử lý |






- Con đường trở thành tỷ phú của 'thần đồng võ thuật' nổi đình đám từ 5 tuổi (29/05/26 21:05)
- Địa điểm vui chơi tránh nóng dịp Tết Thiếu nhi 1/6 tại Hà Nội (29/05/26 20:41)
- Cuộc sống ở nơi cao hơn 5.000m, người dân săn vàng để đổi đời (29/05/26 20:17)
- Con trai lỡ lời, cha đi xét nghiệm ADN và phát hiện mình 'nuôi con tu hú' 22 năm (29/05/26 20:01)
- Từng hạn chế cho dân sở hữu vàng, nay Trung Quốc thay đổi mạnh (29/05/26 19:40)
- Vì sao trung tâm Hà Nội nơi ngập úng, nơi gần như không mưa? (29/05/26 19:21)
- Vietjet và EECO Thái Lan hợp tác xây dựng trung tâm kỹ thuật MRO (29/05/26 19:05)
- Sơn Tùng M-TP hát tiếng Anh thế nào mà gây tranh cãi? (29/05/26 18:41)
- Nắng nóng 'vắt kiệt sức', nhiều người nhập viện vì rối loạn tâm thần (29/05/26 18:21)
- Chủ tịch Hiệp hội Xăng dầu khuyến cáo việc cần làm trước khi chuyển sang dùng xăng E10 (29/05/26 18:02)
Bài đọc nhiều







