Cục trưởng Cục Y tế dự phòng (Bộ Y tế) nêu cơ sở khoa học để tăng thời hạn sử dụng 2 lô vaccine Pfizer (hết hạn ngày 30/11) cho học sinh thêm 3 tháng.
Theo GS.TS Phan Trọng Lân, Cục trưởng Cục Y tế dự phòng (Bộ Y tế), vaccine Pfizer từ ngày 22/8 đã được Cơ quan quản lý dược và thực phẩm Hoa Kỳ (FDA) và Cơ quan quản lý dược Châu Âu (EMA) ngày 10/9 thông qua hạn sử dụng từ 6 tháng lên 9 tháng. Nghĩa là 2 lô vaccine Pfizer 124001 và 123002 nhập về Việt Nam còn hạn sử dụng 3 tháng (từ cuối tháng 10/2021 tăng tới cuối tháng 2/2022).
Áp dụng trên toàn cầu
Ông Lân cho biết, việc tăng hạn sử dụng của vaccine dựa trên kết quả nghiên cứu độ ổn định theo “Hướng dẫn với thuốc mới cũng như sản phẩm sinh học”. Nghiên cứu được thực hiện trên các dải nhiệt độ bảo quản khác nhau, cho thấy vaccine độ ổn định, đảm bảo chất lượng, hạn dùng đến 9 tháng kể từ ngày sản xuất.
Ngoài ra, việc gia hạn áp dụng chung trên toàn cầu và sử dụng cho tất cả đối tượng, gồm trẻ từ 12 tuổi trở lên. Điều này cũng đã được kiểm định khắt khe và đảm bảo chất lượng an toàn, hiệu quả. Các lô vaccine Pfizer hạn sử dụng 6 tháng thì tự động tăng hạn lên 9 tháng sau thời gian FDA và EMA phê duyệt trên.
“Trên cơ sở kết luận của FDA và EMA, ngày 30/9 tại Việt Nam, Hội đồng tư vấn cấp số đăng ký lưu hành thuốc chính thức thông qua kéo dài hạn sử dụng với vaccine của Pfizer từ 6 tháng lên 9 tháng. Tiếp đến, ngày 22/10, Cục Quản lý Dược, Bộ Y tế có văn bản đồng ý về việc tăng hạn dùng của vaccine Pfizer.
Theo đó, các lô vaccine Pfizer được nhập về Việt Nam sau ngày 22/10 với hạn dùng 6 tháng in trên nhãn thì tự động tăng thêm 3 tháng. Như vậy, 2 lô vaccine 124001 và 123002 có hạn dùng đến ngày 28/2/2022”, ông Lân nói.
 |
| GS.TS Phan Trọng Lân, Cục trưởng Cục Y tế dự phòng (Bộ Y tế). |
Cũng theo một lãnh đạo Cục Quản lý dược (Bộ Y tế), trước đây vaccine Pfizer hạn sử dụng là 6 tháng vì nhà sản xuất chưa đủ dữ liệu nghiên cứu và chưa đủ thời gian. Sau này, khi đủ thời gian nghiên cứu, nhà sản xuất kiểm chứng được rằng thay vì 6 tháng thì vaccine Pfizer có hạn sử dụng đến 9 tháng vẫn đảm bảo chất lượng (ở điều kiện bảo quạn nhiệt độ từ - 90 độ C tới – 60 độ C). Việc này được FDA và EMA khẳng định và phê duyệt.
Ngoài ra, trong văn bản của FDA ban hành ngày 23/8 (trước khi 2 lô vaccine Pfizer về Việt Nam sau ngày 22/10) đã hướng dẫn việc tăng hạn sử dụng các lô vaccine của họ thêm 3 tháng (từ 6 lên 9 tháng).
“Trước những dữ liệu trên, Cục Quản lý dược có công văn về việc gia hạn từ 6 tháng lên 9 tháng. Theo hồ sơ được phê duyệt thì dù đến 9 tháng thì vaccine Pfizer vẫn giữ được chất lượng y như 6 tháng. Do đó, các lô vaccine về sau sẽ tự động được gia hạn thêm 3 tháng. Ở Việt Nam, sau khi theo dõi, xem xét chặt chẽ sự thay đổi này trông một thời gian chúng tôi đã quyết định áp dụng từ ngày 22/10. Như vậy, với 2 lô vaccine nhập về từ sau 22/10 sẽ tự động được gia hạn thêm”, vị này cho biết.
Thêm 3 tháng vẫn đảm bảo chất lượng?
Trước băn khoăn của nhiều người về chết lượng và tính an toàn của vaccine gia hạn, PGS.TS Dương Thị Hồng, Phó Viện trưởng Viện Vệ sinh dịch tễ trung ương, Trưởng Văn phòng Tiêm chủng mở rộng Quốc gia cho biết, việc gia hạn sử dụng gần 3 triệu liều vaccine Pfizer thêm 3 tháng là theo hướng dẫn chung của nhà sản xuất, áp dụng trên toàn cầu. Chuyên gia này cũng khẳng định, việc này không ảnh hưởng đến chất lượng của số vaccine trên.
Đại diện Cục Quản lý dược (Bộ Y tế) khẳng định, tất cả các hồ sơ về vaccine Pfizer của hãng đều đã được hãng này kiểm tra nên mới được cấp phép gia hạn. Ngoài ra, khi về Việt Nam, từng lô phải có giấy xuất xưởng của Viện Kiểm định vaccine Quốc gia sau đó mới được đưa ra lưu hành sử dụng. Quá trình sử dụng, những lô vaccine được gia hạn thêm 3 tháng cũng không có gì thay đổi mà vẫn áp dụng đúng theo nguyên tắc thông thường.
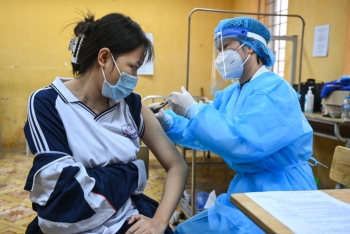
| Vaccine Pfizer được Bộ Y tế chọn để tiêm phòng cho trẻ em tại Việt Nam. |
Liên quan vấn đề trên, đại diện Viện Vệ sinh dịch tễ Trung ương nêu rõ, số vaccine gia hạn thêm 3 tháng theo đề nghị của nhà sản xuất. Cụ thể, ngày 25/11, Viện Vệ sinh dịch tễ Trung ương ban hành quyết định về việc phân bổ vaccine COVID-19 đợt 94. TVới quyết định này, viện cấp 2.960.100 liều vaccine Pfizer gồm 2 lô 124001 và 123002 được mua từ nguồn ngân sách nhà nước cho Trung tâm Kiểm soát bệnh tật (CDC) các tỉnh thành phố để triển khai tiêm chủng cho trẻ em từ 12 - 17 tuổi. Theo thông tin tại giấy chứng nhận xuất xưởng vaccine, sinh phẩm, 2 lô này có hạn sử dụng tới 30/11/2021.
Tuy nhiên, căn cứ vào văn bản ngày 22/10/2021 của Cục Quản lý Dược (Bộ Y tế) về việc tăng hạn dùng của vaccine Comirnaty (Pizer) nhập khẩu về Việt Nam, áp dụng hạn dùng mới 9 tháng với các là vaccine hạn dùng 6 tháng in trên nhãn (tăng 3 tháng hạn dùng so với hạn dùng in trên nhãn, thời gian áp dụng từ ngày 22/10/2021). Văn bản ngày 29/11/2021 của Công ty TNHH Pfizer Việt Nam khẳng định hạn dùng của 2 lô vaccine 124001 và 123002 là ngày 28/2/2022.
Chính vì vậy, Viện Vệ sinh dịch tễ Trung ương đề nghị Trung tâm Kiểm soát bệnh tật các tỉnh, thành phố thông báo tới các đơn vị, điểm tiêm chủng áp dụng hạn mới của vaccine Pfizer nói trên với là 28/2/2022. Đồng thời, các đơn vị cũng cần chỉ đạo các bộ phận y tế tư vấn kỹ cho đối tượng tiêm chủng và cha mẹ trẻ đầy đủ thông tin để tránh hiểu sai về hạn dùng của vaccine nêu trên.
Ngoài ra, Trung tâm Kiểm soát bệnh tật các tỉnh thành phố chỉ đạo các đơn vị khẩn trương tiếp nhận và tổ chức tiêm ngay số vaccine được phân bố cho trẻ em từ 12 đến 17 tuổi trên địa bản. Các đơn vị cũng phải đảm bảo sử dụng vaccine hiệu quả, đúng mục đích, đối tượng, hoàn thành trong thời gian sớm nhất, không để hủy bỏ vaccine do hết hạn sử dụng.
Trước đó, trong văn bản gửi Công ty TNHH Pfizer (Việt Nam) ngày 22/10/2021 về việc tăng hạn dùng của vaccine Comirnaty, Cục Quản lý Dược (Bộ Y tế) đồng ý về việc tăng hạn sử dụng vaccine Comirnaty từ 6 tháng lên 9 tháng ở điều kiện nhiệt độ bảo quản từ - 90 độ C đến - 60 độ C. Theo Cục Quản lý Dược, công ty Pfizer (Việt Nam) chịu trách nhiệm về chất lượng với vaccine đang lưu hành trên thị trường và trách nhiệm thông báo sự thay đối này đến các đơn vị có liên quan.
Cục Quản lý Dược cũng đề nghị Công ty TNHH (Pfizer) Việt Nam tiếp tục cập nhật, cung cấp các kết quả nghiên cứu tính ổn định còn thiếu của ít nhất 3 lô tại các cơ sở sản xuất vaccine Comirnaty khác trong vòng 30 ngày kể từ khi có kết quả nghiên cứu tính ổn định đến 9 tháng.
Trong vòng 6 tháng kể từ ngày ký công văn này, Công ty TNHH Pfizer Việt Nam được áp dụng hạn dùng mới 9 tháng đối với các lô vaccine sẽ được nhập khẩu vào Việt Nam với hạn dùng 6 tháng in trên nhãn (tăng 3 tháng hạn dùng so với hạn dùng in trên nhãn).
Ngày 12/6, vaccine Comirnaty của Pfizer được Bộ Y tế phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch bệnh COVID-19.
Từ đầu tháng 11, Bộ Y tế quyết định triển khai chiến dịch tiêm chủng vaccine COVID-19 cho trẻ em trên toàn quốc với vaccine được chọn là Pfizer.
PHẠM QUÝ
 Hà Nội dừng tiêm 2 lô vaccine Pfizer vừa được gia hạn thêm 3 tháng Hà Nội dừng tiêm 2 lô vaccine Pfizer vừa được gia hạn thêm 3 tháng |
 Vì sao Bộ Y tế gia hạn sử dụng vaccine Pfizer? Vì sao Bộ Y tế gia hạn sử dụng vaccine Pfizer? |
 Bộ Y tế lên tiếng về việc gia hạn thêm 3 tháng 2 lô vaccine Pfizer Bộ Y tế lên tiếng về việc gia hạn thêm 3 tháng 2 lô vaccine Pfizer |
Ngày đăng: 16:15 | 01/12/2021
/ vtc.vn